Fe³⁺与Cu²⁺催化H₂O₂分解效果的比较实验分析
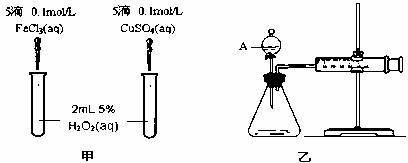
题目描述了一项比较Fe³⁺和Cu²⁺对过氧化氢(H₂O₂)分解催化效果的实验研究。实验中设计了甲、乙两种装置,并提出了相关问题。以下是对题目中两个问题的具体分析与解答。
(1) 观察指标与试剂改进的合理性
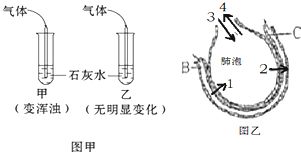
如图甲所示的实验,是通过观察 反应产生气泡的快慢 来比较Fe³⁺和Cu²⁺的催化效果。这是因为H₂O₂在催化剂作用下分解的产物是水和氧气,反应速率越快,单位时间内产生的氧气气泡就越多、越密集,从而可以通过视觉直观地比较气泡产生的速率来定性判断催化剂的催化效率。
题目中提到,有同学建议将催化剂FeCl₃改为Fe₂(SO₄)₃更为合理。这一建议的核心理由是 控制阴离子相同,排除阴离子的干扰。
在对比实验中,为了确保实验结论的准确性,必须遵循“控制变量”的原则。本实验旨在比较不同金属阳离子(Fe³⁺和Cu²⁺)的催化作用,那么其他可能影响反应速率的因素应尽可能保持一致。如果使用FeCl₃和CuSO₄,那么体系中同时存在Cl⁻和SO₄²⁻两种不同的阴离子。理论上,这些阴离子本身也可能对H₂O₂的分解产生微弱影响,或者与金属离子形成不同性质的配合物而间接影响催化活性。使用Fe₂(SO₄)₃后,Fe³⁺和Cu²⁺的催化反应都在硫酸根离子的环境中进行,从而排除了因阴离子种类不同而可能带来的干扰,使实验对比更纯粹,结论更可靠。
(2) H₂O₂在二氧化锰作用下反应的化学方程式
题目中还要求写出H₂O₂在二氧化锰(MnO₂)催化作用下发生反应的化学方程式。二氧化锰是过氧化氢分解最经典、最常用的催化剂之一。该反应的化学方程式为:
2H₂O₂ MnO₂→ 2H₂O + O₂↑
这是一个分解反应,二氧化锰作为催化剂,其本身在反应前后的质量和化学性质不变,它降低了反应的活化能,加快了过氧化氢分解为水和氧气的速率。书写时应注意标明催化剂MnO₂以及氧气的气体符号“↑”。
本题综合考查了对照实验的设计思想、控制变量法的应用以及对常见催化反应方程式的掌握。通过观察气泡产生速率进行定性比较,是化学实验中判断气体产生型反应快慢的常用方法。而在设计对比实验时,确保除待研究变量外其他条件一致,是得出科学结论的基础。将FeCl₃换为Fe₂(SO₄)₃,正是这一科学思维的体现。