牙膏中碳酸钙含量的探究实验设计与分析
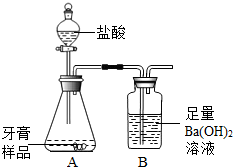
化学兴趣小组针对某品牌牙膏中碳酸钙含量的测定展开了科学探究。根据资料显示,该牙膏的摩擦剂主要由碳酸钙和氢氧化铝组成,且其他成分与盐酸反应时不产生气体。以下为实验设计与分析过程。
一、实验原理
牙膏中的碳酸钙可与稀盐酸反应生成二氧化碳气体,而氢氧化铝虽能与酸反应,但不产生气体。通过测量反应生成的二氧化碳质量或体积,可以计算出碳酸钙的含量。化学方程式为:
CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑
二、实验装置与步骤
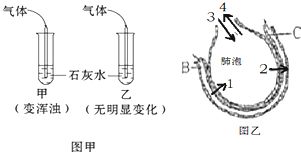
实验采用上图所示装置(图中含夹持仪器、干燥管、吸收瓶等),主要步骤如下:
- 称取一定质量的牙膏样品,置于反应瓶中。
- 向反应瓶中加入足量稀盐酸,确保碳酸钙完全反应。
- 反应生成的气体经干燥后,被装有碱石灰(或氢氧化钠溶液)的吸收装置完全吸收。
- 测量吸收装置在反应前后的质量差,即为生成的二氧化碳质量。
三、数据记录与计算
假设实验数据如下:
- 牙膏样品质量:m₁ g
- 吸收装置增加的质量(CO₂质量):m₂ g
通过化学方程式计算碳酸钙的质量:
设碳酸钙质量为 x,则有:
100 / x = 44 / m₂
x = (100 × m₂) / 44
碳酸钙的质量分数为:
(x / m₁) × 100%
四、误差分析
实验可能产生误差的因素包括:
- 装置中残留的二氧化碳未被完全吸收,导致结果偏低。
- 空气中的二氧化碳或水蒸气干扰吸收装置,需设置干燥管和空白对照。
- 盐酸可能挥发,需使用足量但不过量的酸。
五、实验结论
通过测定二氧化碳质量,结合化学计算,可准确得出牙膏中碳酸钙的含量。该方法操作简便,适用于日常化学探究,有助于理解定量分析在生活中的应用。
六、拓展思考
若要进一步区分碳酸钙和氢氧化铝各自含量,可设计后续实验,如利用氢氧化铝与碱反应的性质进行分离测定。此探究体现了化学实验在产品质量分析中的实用价值。